编者按:在日前举行的2021年ESMO靶向抗癌治疗(ESMO TAT)会议上,一项来自英国的单中心回顾性研究提示,既往存在自身免疫性疾病的癌症患者与非AID的癌症患者相比,使用免疫检查点抑制剂(ICIs)治疗后的免疫相关不良事件(irAE)并无显著差异[1]。
自身免疫性疾病(Autoimmune disease,AID)是指自身免疫反应导致组织器官或功能障碍的疾病。临床上有许多疾病都别归类为AID,如自身免疫性肝炎、甲状腺功能亢进、Ⅰ型糖尿病、溃疡性结肠炎、系统性红斑狼疮、类风湿关节炎、系统性血管炎硬皮病等。另一方面,AID的流行率也呈上升趋势,一项调查研究显示,2011~2012年美国的抗核抗体(ANA)阳性率达到15.9%,约4100万人受此影响[2]。
免疫检查点抑制(ICIs)通过“松开免疫刹车”(阻断PD-1/PD-L1、CTLA-4等肿瘤免疫逃逸的分子靶点),从而恢复自身免疫系统的抗肿瘤能力,其治疗原理有所雷同于AID的致病机制。在ICIs的临床试验和实践中,免疫相关不良事件(irAE)也越来越受到关注。那么,当AID患者罹患癌症,ICIs治疗会不会“火上浇油”,使患者发生更严重的irAE?来自伦敦大学学院医院的Grisma Patel教授团队进行了一项单中心的回顾性分析[1],总结了2017年1月至2020年12月期间562例使用ICIs治疗的患者特征,其中有15例既往存在AID。将AID和非AID进行匹配(1:3),以比较两组患者的irAE特征和疗效。
15例既往存在AID的患者中,有炎症性肠病5例,银屑病3例,类风湿性关节炎或风湿性多肌痛各2例,自身免疫性内分泌病4例,狼疮或结节病各1例,2例合并2种AID。这些患者的AID疾病得到良好控制,其中有9例接受激素替代治疗、外用药物治疗,3例接受免疫抑制治疗(其中2例接受<10 mg的泼尼松龙治疗,1例接受美沙拉秦治疗);另有6例没有接受AID治疗。
AID和非AID患者均接受妇科肿瘤、结直肠癌、头颈癌、Merkel细胞癌、尿路上皮癌或非小细胞肺癌的相关抗肿瘤治疗。
AID队列中和非AID队列中分别有4例和13例患者接受临床研究的ICIs治疗,另外分别有11例和32例患者接受临床研究外的ICIs治疗。AID队列和非AID队列中大多数患者(分别为9例和27例)接受了帕博利珠单抗治疗,此外还有纳武利尤单抗(2例和6例)、纳武利尤单抗+伊匹木单抗(2例和6例)、阿替利珠单抗(1例和3例)、度伐利尤单抗(1例和3例)。
通过ICIs治疗,AID队列中的15例患者中有3例经历了可能与其潜在AID相关的irAE;这3例患者分别为银屑病、类风湿性关节炎和结肠炎。
AID(n=15)和非AID(n=45)的匹配患者队列中,两组患者的irAE事件数(6/15 vs 27/45,P=0.5691)无显著差异,其中AID和非AID组分别有9例和21例未发生irAE,5例和17例仅有一个irAE,1例和7例经历了2个irAE。此外,两组患者3-5级irAE发生率数(1/15 vs 9/45,P=0.42)也没有现显著差异。
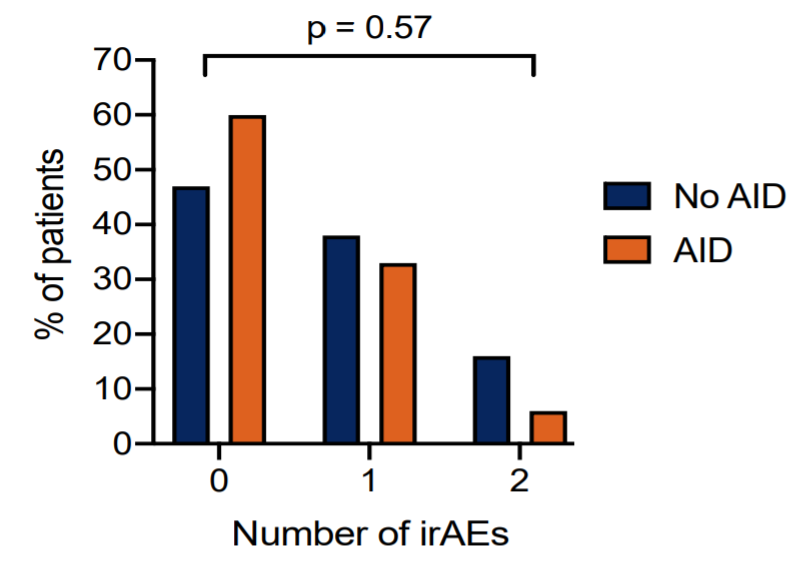
▲两组患者的irAE事件比例
同样地,两组间的最佳治疗反应无显著差异(P=0.91)。在AID和非AID队列中,分别有7例和18例患者获得完全或部分缓解(CR/PR),1例和5例患者为混合缓解(MR),2例和5例患者为病情稳定(SD),4例和15例患者出现病情进展(PD)。
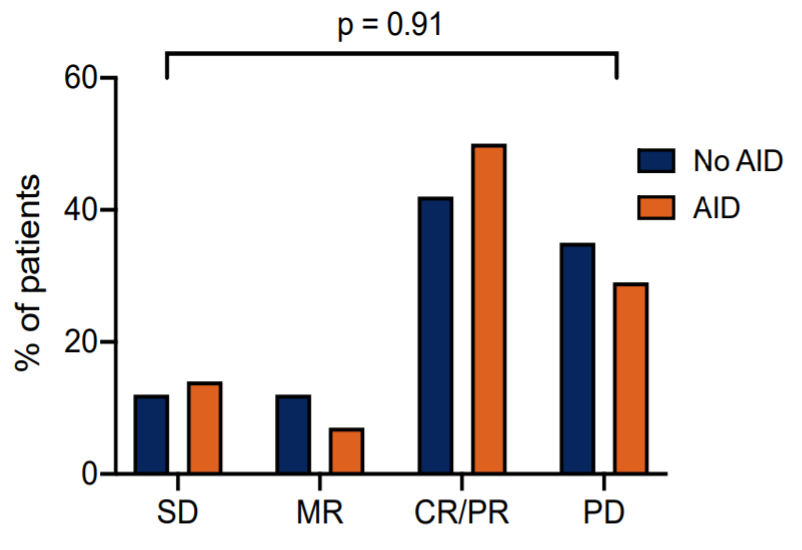
▲两组患者的疗效比例
根据该三级癌症中心ICIs治疗患者的电子记录证据,作者得出结论认为,在包含几个不同ICIs的治疗中,既往存在的AID患者病情恶化并不频繁,也不会导致严重的毒性。研究者认为AID控制良好的患者可以考虑纳入ICIs的临床研究中。[1]31P–Patel G, Sawhney P, Ohana D, et al. Safety and efficacy of immune checkpoint inhibitors in cancer patients with pre-existing autoimmune disease: A UK tertiary cancer centre experience. ESMO Targeted Anticancer Therapies (TAT) Virtual Congress (1-2 March 2021).[2]令人担忧:美国自身免疫性疾病发病率日渐攀升!. 国际糖尿病. https://mp.weixin.qq.com/s/BPM24rRiJSwBRzu1zC8xJg 




 京公网安备 11010502033352号
京公网安备 11010502033352号