一项关于晚期骨髓纤维化的LSD1抑制剂IMG7289(bomedemstat)的II期研究
旨在研究MF患者中IMG-7289的疗效及安全性。
本研究患者每日口服IMG-7289,起始剂量0.25mg;每周滴定血小板控制在(50-100)×109/L;周期为84天;每周期后2-4周洗脱期。IIb期研究设定设定目标人群每日口服IMG-7289,起始剂量0. 5mg/kg;每3周滴定血小板控制在(50-75)×109/L;周期为168天。
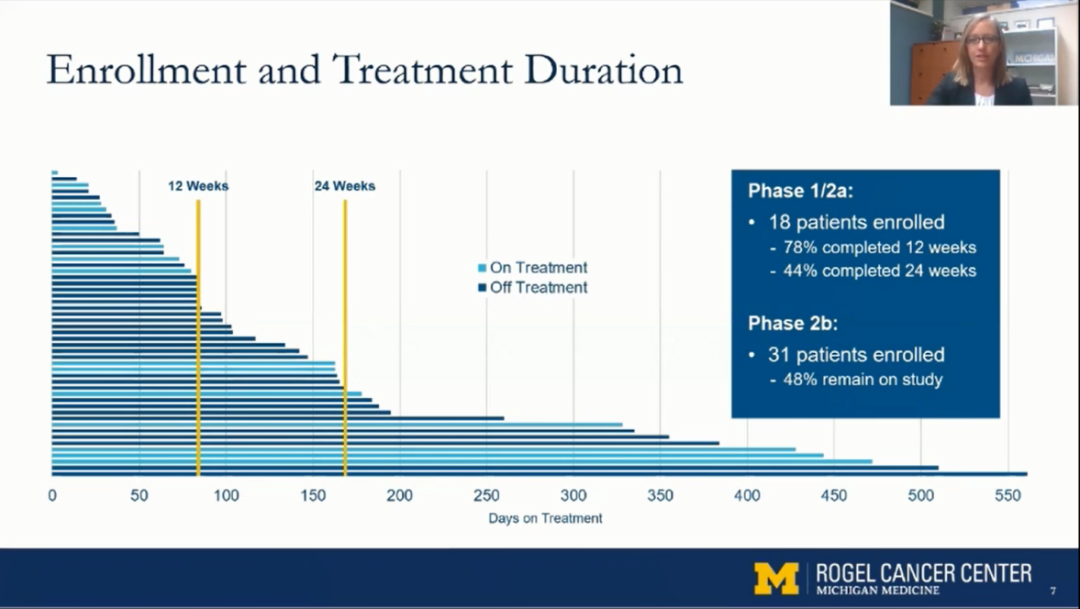
共纳入49例患者,包括49%PMF,36%PET-MF,15%PPV-MF。中位年龄是68(范围34-88)岁。IPSS评分中危占45%,高危占55%。男性占55%,女性占45%。I/IIa期共18入组例患者,78%完成了12周,44%完成了24周;
IIb期共纳入31例患者。除1名患者外,其他所有患者先前都接受过芦可替尼治疗;65%的人接受了多达4种额外的治疗,包括fedratinib和CPI-0610。37%的患者在基线时依赖输血。62%为IPSS高风险,其余为中风险。中位治疗时间为110(21-561)天。
有效性方面:在第12周所有可评估总症状评分(TSS)的32例患者中,78%(25例)有TSS评分改善,其中25%(8例)TSS减少≥50%;在第12周入组2b期的14例患者中,86%(12例)出现脾脏体积的减少,14%(2例)脾脏体积减少≥35%,29%(4例)脾脏体积减少≥20%,没有转化为AML的病例。对22例患者49个不同变异等位基因频率(VAF)进行连续追踪,VAF降低32%,稳定55%。与CALR和MPL相比,JAK2突变的细胞对治疗更敏感;ASXL1突变的克隆对IMG-7289的敏感性最高。所有患者均未发现新的突变。
安全性方面:38例(95%)报告771例不良事件,其中33例为SAEs。被认为可能与IMG-7289有关主要不良反应为:脾肿痛、直肠出血、心力衰竭和头痛。亦无无剂量限制性毒性、药物相管的死亡或发展为AML。

IMG-7289在晚期MF患者中安全且耐受性良好;IMG-7289单药治疗晚期MF患者具有临床有效:临床症状、脾脏体积、贫血、骨髓纤维化不同程度改善;IMG-7289能减少1/3VAF,尤其是ASXL1突变;治疗期间无新的基因突变或进展为AML。
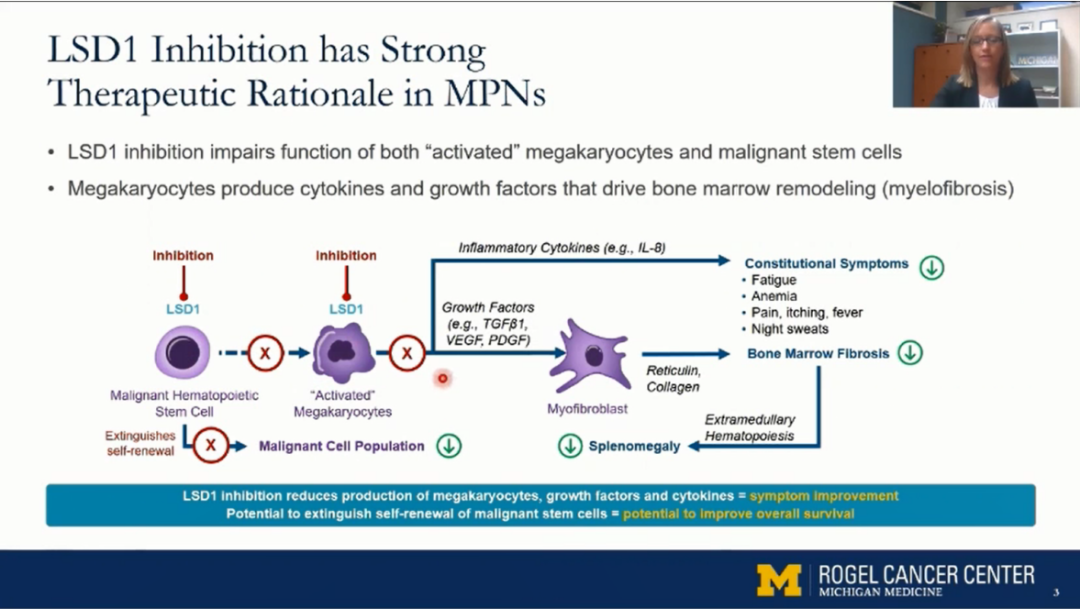
LSD1是一种对巨核细胞的成熟和正常活动以及恶性造血干/祖细胞的自我更新至关重要的表观遗传修饰酶,被认为是骨髓纤维化(MF)的致病生长因子和细胞因子的主要来源。IMG-7289(Bomedemstat)作为口服小分子LSD1抑制剂,主要通过同时增加P53的表达和甲基化、独立地通过促凋亡因子PUMA并降低抗凋亡拮抗剂BCLXL的水平,选择性抑制JAK2V617F细胞的增殖并诱导其凋亡,因此其在MF患者的治疗中理论上是可行的,前期前临床试验也为其提供了依据。本项研究显示了口服药物IMG-7289可改变晚期MF患者症状、脾脏体积、贫血、骨髓纤维化,减少1/3患者的等位基因突变频率,尤其是ASXL1,表现出良好的安全性、有效性和耐受性,后期可在前临床试验及此试验基础上进一步对ET和PV患者进行研究,此外针对IMG-7289联合 芦可替尼对MPN的研究也是一个新的方向。
二、#52.The Addition of Navitoclax to 芦可替尼 Demonstrates Efficacy within Different High-Risk Populations in Patients with Relapsed/Refractory Myelofibrosis.
Navitoclax与芦可替尼的合用在不同高危人群中对复发/难治性骨髓纤维化患者有效。
Navitoclax是一种新的口服的抗凋亡蛋白 BCL-XL和BCL-2抑制剂。临床前的研究显示:JAK2和BCL-XL/BCL-2抑制剂联用,可以克服获得性JAK抑制剂耐药。既往对芦可替尼没有反应的骨髓纤维化(MF)患者,治疗选择有限。navitoclax (Nav)和 芦可替尼 (NCT03222609)的联用,对不再受益于 芦可替尼的MF患者,可诱导有临床意义的脾脏体积(SVR)应答、总症状评分(TSS)改善和骨髓纤维化(BMF)分级降低。本II期临床研究旨在评估1.HMR的存在或研究开始时突变的基因总数是否与临床结果(SV降低≥35%[SVR35]、TSS和BMF降低)和驱动基因(JAK2 p.V617F和突变的CALR)变异等位基因频率(VAF)降低相关。2.评估Nav+ 芦可替尼是否能改变MF炎性细胞因子水平及后者与临床结果的相关性。
接受连续芦可替尼治疗≥12周且有持续性脾肿大,需要新的Tx治疗的MF患者被纳入。患者继续使用芦可替尼,Navitoclax从每日50 mg开始,在耐受基础上逐步增加到300 mg。研究终点包括SVR35(MRI)、第24周TSS (MF症状评估表4.0版)和BMF的变化。在基线和第24周,通过NGS测序外周血54个髓系肿瘤组合基因,对外周血进行突变分析,包括VAF测定。在基线,第12周和第24周,使用133种分析物组合测量血浆中的炎症细胞因子水平。

截至2020年2月28日,共纳入34例MF患者接受了≥1剂量Navitoclax+ 芦可替尼治疗。进入研究时,33名患者可进行生物标志物分析。26/33例(79%)患者中出现JAK2突变,7/33例(21%)患者CALR突变阳性。JAK2和CALR突变的患者中位VAFs分别为88%和39%。基线突变分析显示,19/33(58%)名患者中存在HMR基因突变;其中8/19 (42%)HMR基因突变≥2个。ASXL1、SRSF2、EZH2、U2AF1和IDH1的突变率分别为13/19(68%)、7/19(37%)、4/19(21%)、2/19(10%)和1/19(5%)(图1)。在基线检查时,所有突变基因的中位数为3,17/33(52%)的pts具有≥3个突变。
在治疗第24周,9/34(27%)达到SVR35, 6/20(30%) TSS (TSS50)降低≥50%,7/34 (21%)BMF有-1/-2级改善,12/26(46%)>有10%的驱动基因VAF减少。观察到第24周的临床反应和VAF减少与HMR突变的存在和突变的基因数量无关。进一步的分析发现β-2微球蛋白(B2M),肿瘤坏死因子受体2(TNFR2)、金属蛋白酶组织抑制剂1 (TIMP-1)和血管细胞粘附分子1(VCAM-1)4种细胞因子与TSS的改善有关。
既往接受过芦可替尼治疗的MF患者,随后接受Navitoclax和芦可替尼联合治疗,可获得有临床意义的SVR、TSS改善、BMF降低和驱动基因VAF减少,这些与HMR突变和突变基因总数无关。细胞因子分析表明,Nav + 芦可替尼联合应用可能在改善关键细胞因子方面发挥作用,这些细胞因子参与了单纯 芦可替尼反应不佳的MF患者TSS的改善。
MF(骨髓纤维化)是一种主要由JAK/STAT信号驱动的骨髓增殖性肿瘤,伴随着生长转录因子、炎性因子、抗凋亡蛋白BCL-XL等的增加。很多患者在JAK抑制剂治疗后复发,长期有效药物有限;具有高分子风险(HMR)突变(定义为ASXL1、SRSF2、EZH2、U2AF1和IDH1/2突变)的MF患者的总生存期缩短和/或白血病转化风险也同时会增加增加。在对芦可替尼失去反应的骨髓纤维化(MF)患者中,navitoclax和 芦可替尼 (NCT03222609)的联合应用,在不再受益于 芦可替尼的MF患者中,可诱导有临床意义的脾脏体积(SVR)应答、总症状评分(TSS)改善和骨髓纤维化(BMF)分级降低。但这些与VAF减少与HMR突变的存在和突变的基因数量无关。正在进行的细胞因子分析表明,navitoclax+ 芦可替尼联合应用可能在改善关键细胞因子方面发挥作用,这些细胞因子参与了单纯 芦可替尼反应不佳的MF患者TSS的改善。
三、#53.Favorable Overall Survival with Imetelstat Treatment Correlates with Other Clinical Benefits in Intermediate 2 or High Risk Myelofibrosis Relapsed/Refractory to Janus Kinase Inhibitor
Janus激酶抑制剂复发或耐药的中危-2或高危骨髓纤维化患者中,Imetelstat治疗的良好总生存与其他临床获益相关骨髓纤维化(MF)是一种严重且危及生命的骨髓增殖性肿瘤。目前,对于Janus激酶抑制剂(JAKi)治疗后复发或难治的患者尚无获批的治疗选择,总生存期(OS)不佳(范围:13-16个月)。
本研究旨在评估Imetelstat(一种端粒酶抑制剂)针对JAKi R/R的MF患者接受9.4 mg/kg 剂量的OS改善效果。

IMbark(MYF2001;NCT02426086)是一项随机、单盲、2期研究,研究对象为R/R中危2/高危MF患者,每3周静脉注射一次imetelstat 9.4 mg/kg或4.7 mg/kg,评估两个剂量下:剂量相关性临床获益,症状反应和OS获益。主要终点为24周时脾脏反应和症状缓解率。OS是一个关键的次要终点。骨髓纤维化由中心病理学家评估。所有相关分析都不是预先规定的,而是探索性的。
所有107例入组患者(9.4 mg/kg组n=59,4.7 mg/kg组n=48)均纳入ITT分析。截至2020年2月19日,中位随访时间为41.7个月,9.4 mg/kg组的中位OS为28.1个月(95%CI 22.8-31.6),4.7 mg/kg组为19.9个月(95%CI 17.1-33.9)(图1)。
在第24周达到症状反应的患者,与未达到症状缓解或未评估的患者相比,具有更长的OS趋势(HR = 0.79,95%CI 0.41-1.51)。在第24周达到脾脏反应的患者中观察到相似趋势(HR = 0.46,95%CI 0.11-1.92)。此外,与≤20%SVR降低相比,≥20%SVR与更好的OS趋势相关(HR = 0.44,95%CI 0.19-1.04)。SVR临界值≥10%时趋势仍然存在(HR = 0.69,95%CI 0.38-1.27),与已发表的数据一致。在有骨髓资料的57例患者中,19例患者(33%)在研究期间骨髓纤维化改善≥1度,OS显著长于骨髓纤维化恶化的患者(HR = 0.36,95%CI 0.13-0.96 p = 0.04)。在纤维化稳定与恶化的30例患者(53%)中观察到相似趋势(HR = 0.47,95%CI 0.19-1.20)。
一些基线疾病特征因素被确定为生存的预后因素,与治疗剂量无关。治疗前DIPSS高风险、ECOG体能状态、输血依赖性、基线中性粒细胞升高、基线Hb和血小板值降低,均与死亡风险增加相关。
这些数据显示,在JAKi R/R MF患者中,imetelstat可使OS出现剂量相关改善。与其他临床获益相关的趋势支持使用imetelstat观察到的潜在生存获益,值得进一步临床研究。
Imetelstat已在IMbark临床试验中证明了症状反应和OS潜在改善方面的临床获益,这是一项在对JAKi R/R的MF患者中进行的2期临床研究。IMbark 研究的总生存期结果与imetelstat治疗观察到的临床获益具有相关性。imetelstat可使OS出现剂量相关改善,相关性分析显示,第24周达到症状缓解、脾脏体积减少范围 > 10%及 > 35%以上的患者的OS均有延长趋势,骨髓纤维化改善患者的OS有统计学显著改善。总体而言,这些结果支持对R/R中危-2/高危MF患者行imetelstat治疗。
兰州总医院血液科 副主任 博士,研究生导师
学术任职:
中华医学会血液学分会 委员
全军血液专业委员会青委会 副主任委员
中国整合医学协会血液学分会 委员
获奖国家级、省(部)级奖项5项。承担国家自然科学基金、军队重点科研课题及甘肃省自然科学基金多项。





 京公网安备 11010502033352号
京公网安备 11010502033352号